
A modern anesztézia célja adekvát analgézia
|
IX./6. fejezet: A genetikai tesztek értelmezésének gyakorlati nehézségei
A sikeres tesztelés kapcsán a pozitív diagnosztikai eredmények közlése személyes találkozás keretében történik. Fontos előfeltétel a háttér pontos ismerete, hogyan kapcsolódik a gén a betegséghez, illetve milyen bizonytalanságok árnyalhatják a képet. A pozitív lelet orvosi és genetikai következményeit megvilágítva tisztázni kell, az eredmények ismerete hogyan befolyásolhatja az egyén és családja életét (ld. Genetikai tanácsadás fejezet).
Mint minden laboratóriumi eljárás esetében, a genetikai tesztek kapcsán is különös figyelmet kell fordítanunk a méréstechnikai bizonytalanságokra. A diagnosztikai célú eljárások elfogadható analitikai szenzitivitás és specificitás mellett, a laboratóriumoknak minőségbiztosítási standardoknak, akkreditációnak, sőt a munkafolyamatoknak rendszeres körvalidációkon (proficiency testing) is meg kell felelniük. Az újgenerációs szekvenálás eredményeinek kapcsán számos egyéb méréstechnikai paramétert is figyelembe kell vennünk a megfelelő értelmezés érdekében (utóbbiról és a genetikai lelet felépítéséről részletesen ld. a WES/WGS fejezetben).
A genetikai vizsgálatok során azonosított, különösen szekvenciaszintű eltéréseket klinikai/kóroki jelentőség szerint egy ötfokozatú skálán helyezhetjük el. (NB. A kauzalitás, a genetikai eltérés magyarázza a állapotot, mint okozatot, nem egyenlő a várható funkcionális károsító hatással (damaging, deleterious, high-impact mutation). A „betegséget okozó” kóroki (patogén), illetve a funkcionális, pl. biokémiailag nem-semleges következménnyel bíró fogalmak között különbségek vannak: minden kóroki variáns károsító, de nem minden károsító kóroki.)
|

Hogyan értékeljük a genetikai variánsok és a velük összefüggésbe hozott állapotokra vonatkozó bizonyítékokat?
|
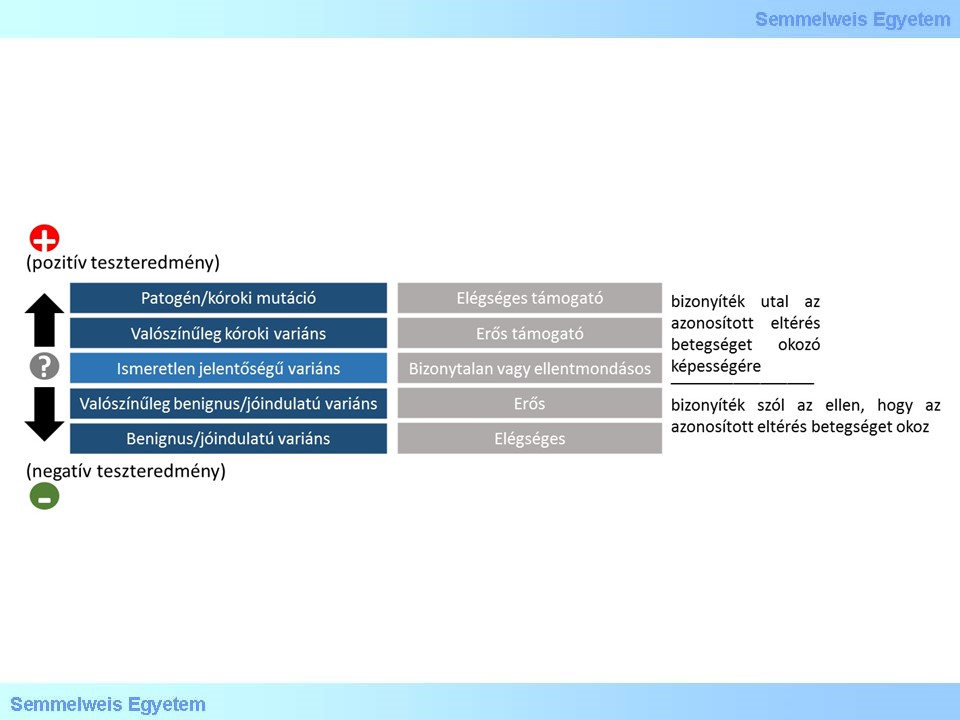
13. ábra: A genetikai variánsok és adott fenotípus, rendellenesség vagy betegség közötti összefüggés megbízhatóságát leíró skála
|
Az ACMG (American College of Medical Genetics) munkacsoportja által javasolt és jelenleg elterjedt séma a variánsok klinikai jelentőség szerinti besorolásra. Két további kategória a „patogén (alacsony penetranciával)” és a „pszeudodeficiencia allél”.
A variánsok klinikai jelentőséghez rendelése során, variáns klasszifikációjában használatos további kódok:
-
- gyógyszerre adott válasz (drug response): A variáns egy gyógyszerre adott választ befolyásol, nem egy betegség kialakulását,
-
- asszociáció (association): a genomszintű asszociációs vizsgálatok (GWAS) során azonosított eltérések,
-
- rizikótényező (risk factor): a betegséget önállóan nem okozó variánsok, amelyek jelenléte azonban az adott betegség kockázatát növeli,
-
- védő faktor (protective): adott rendellenesség, fertőzés kockázata csökkent a variáns jelenlétében,
-
- hatással van (Affects): azon variánsokra fenntartott címke, amelyekkel összefüggésbe hozott fenotípus nem minősül betegségnek, mint pl. laktóz intolerancia, továbbá
-
- számos egyéb címke, mint conflicting data from submitters, other, not provided…
|

…hogy a leletek értékelésekor gondoljuk át, hogy a megfigyelt tünetek, rendellenességek magyarázhatóak-e a detektált genetikai eltéréssel.
|
Pozitív eredményről beszélünk tehát, ha sikerül a beteg állapotát okozó genetikai hibát a megfelelő módszerrel és minőségben végrehajtott vizsgálat segítségével.
Feltétel természetesen, hogy a variáns a megfelelő zigozitással legyen jelen: egy autoszomális recesszív formában ismert betegség esetében az érintett génben mindkét allélon homozigóta vagy komplex (vagy más néven compound) heterozigóta formában várjuk el a funkcióvesztő variáns megjelenését. Ritka esetben a két allélon eltérő típusú mutáció mutatható ki, misszenz mutáció kombinálódhat egy a bázissorrend elemzése során nem észlelhető génátrendeződéssel.

14. ábra: Bármely genetikai eltérésnek a fenotípushoz való ok-okozati viszonyának értékelésekor mérlegelhető szempontok
|
IX./6.1. Az azonosított szekvencia eltérések értelmezésének lépései
|

Mit gondoljunk át a negatív leletekkel kapcsolatban? Kell-e foglalkoznunk az ismeretlen jelentőségű variánsokkal?
|
A leletek értelmezése során gyakran találkozunk olyan esetekkel, amikor ismeretlen klinikai jelentőségű variánst azonosítunk egy génben, amelynek funkcióvesztő mutációja ugyan a beteg megfigyelhető fenotípusát jól magyarázhatná, bizonyítékok (több független megfigyelés a variáns és a betegségállapot együttes megjelenéséről) hiányában mégsem nyilatkozhatunk egyértelműen annak kóroki voltáról. Ebben az esetben a mutációnak a fehérje-kódoló génben való elhelyezkedése alapján következtethetünk jelenlétének várható következményeire. A szekvenálási adatok elemzése során legnagyobb variáns típus, a misszenz pontmutációk esetén egész sor gépi tanulást alkalmazó algoritmus érhető el a non-szinonim variánsok funkcionális predikciójára (ld. a WES/WGS fejezetben), amelyek segítségével megbecsülhető az eltérés várható hatáserőssége.
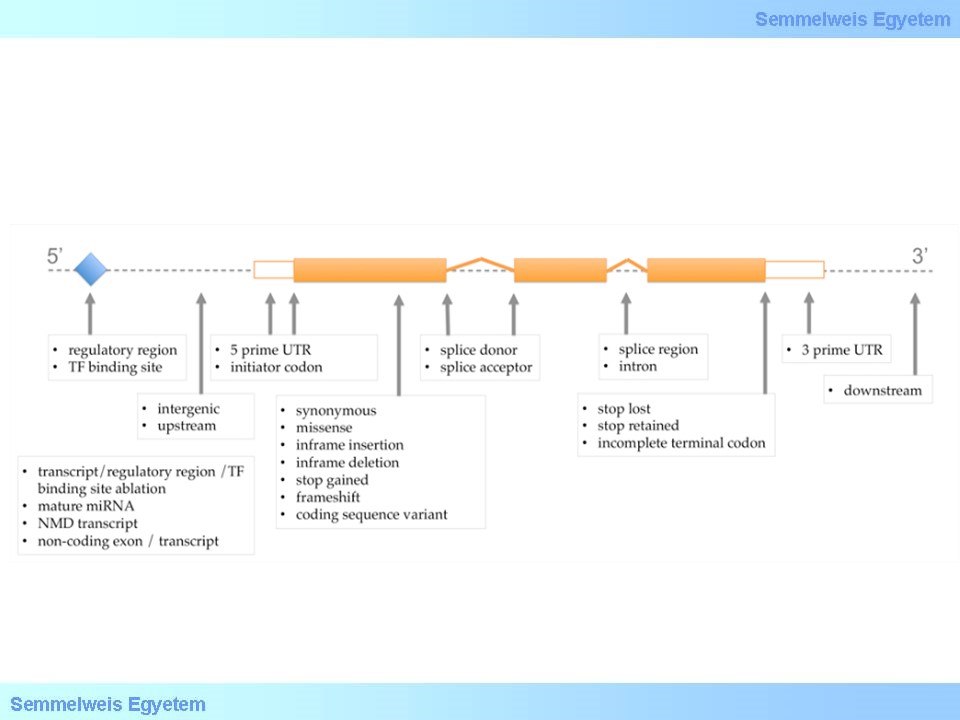
15. ábra: A mutációk elhelyezkedése alapján besorolható típusok. Forrás és jelmagyarázat: Ensembl Genome Browser honlapján
|
Legalább ilyen fontos végiggondolni a jóval gyakoribb helyzetet, ha a teszt nem jár sikerrel és nem találunk az egészségi állapotot magyarázó genetikai tényezőt.
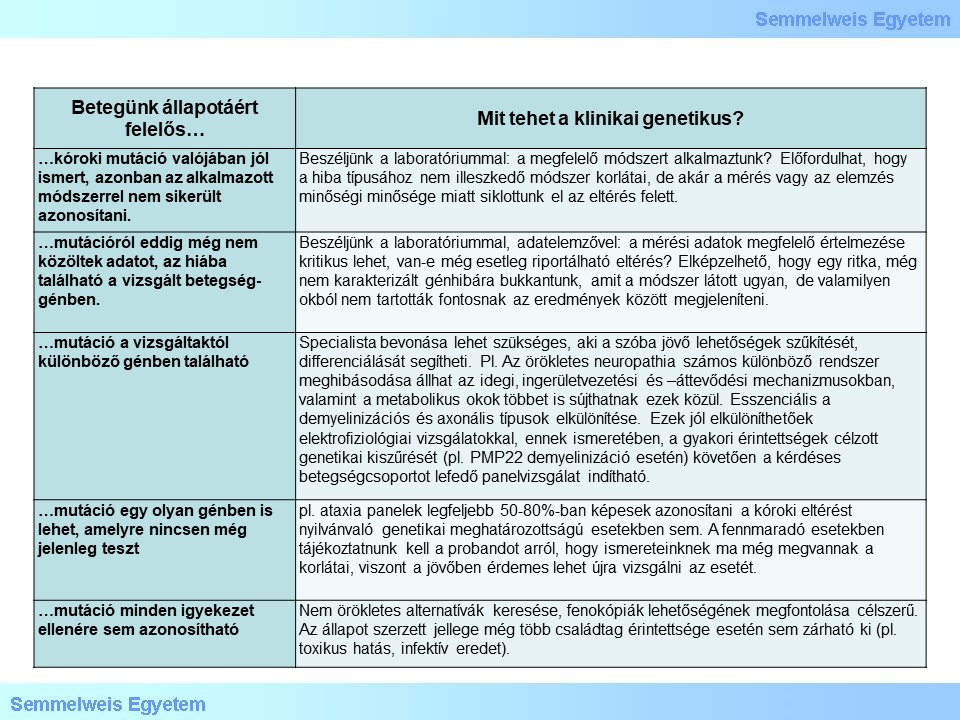
5. táblázat: A negatív genetikai leletek lehetséges olvasatai
|
Az ismeretlen jelentőségű variánsok (VUS: variant with unknown significance) jellemzője, hogy rendelkeznek egy önállóan betegséget kiváltani képes mutáció tulajdonságaival, de klinikai jelentőségét illetően elégtelen vagy ellentmondó bizonyíték érhető el.
|

Mit jelent a reklasszifikáció és az újraértékelés?
|
Főbb VUS értékelési szempontok, amelyet egyedi esetekben is elvárhatunk, hogy a variáns:
-
- jellemzően ritka,
-
- gyakran evolúciósan konzervált szakaszon, illetve funkcionális domént károsíthat, jelentősen befolyásolhatja a fehérje térszerkezetét stb.), és
-
- az érintett gén kapcsolatba hozható a beteg fenotípusával.
Ha a betegség több családtagot érint a családban és valószínűsíthető egy adott VUS szerepe, a családtagok célzott tesztelése igen hasznos lehet. A szegregációs vizsgálat rendszerint segíthet a szükséges információk megszerzéséhez, ahol azt várjuk el, hogy a valószínűsíthetően patogén variáns az érintett családtagokban is kimutatható legyen. Recesszív rendellenességekben szenvedő probandok esetében keressük a szülőkben az érintett gén variánsait. A mindkét allélon kialakuló de novo mutációk ilyen esetekben igen ritkák, ha mégis látjuk, inkább mérési hibára gondoljunk.
Előfordul, hogy egy variáns klinikai jelentőségét egy új tanulmány alapján vagy adatbázisba történő adatszolgáltatáshoz kapcsolódóan felülvizsgálják, így az egy másik osztályba kerül (tipikusan VUS > patogén). Nehéz megjósolni, hogy mikor gyűlik össze elég bizonyíték egy adott pozícióval kapcsolatban, az a variáns és a betegség előfordulási gyakoriságától és a kapcsolódó kutatások aktivitásától is függ. Így az is előfordul, hogy a genetikai vizsgálatok mérési adatai csak a jövőben kerülhetnek megfelelő megvilágításba, ezért a megoldatlan esetekben talált eltérések státuszát időről időre újra értékelni lenne szükséges, számítva azok esetleges reklasszifikációjára.
|
|