| |
VII./2.3.: Meningeom
VII./2.3.1.: Begriffsdefinition
|
| |
Das Meningeom ist solch ein extraaxialer Tumor (nicht im Gehirnparenchym lokalisiert), der aus speziellen meningothelialen Deckzellen und trabekulären Zellelementen, die die Arachnoidea bilden, entspringt.
Die intraduralen Sinuse und ihre Anhangsgebilde, sowie der Plexus choroideus werden ebenfalls von meningothelialen Zellen bedeckt.
VII./2.3.2.: Eigenschaften der meningothelialen Zellen (mit der etwas veränderten Aufzählung von Perry et al.2004))
VII./2.3.2.1.: Aeusseres Erscheinen
|
 |
Meningotheliale Zellen besitzen die Eigenschaft, dass sie sich um sich herum, oder um andere Strukturen (austretende Nervenzellen, Gefässe) herum wringen und dadurch eine Art Barriere bilden. Sie sind durch Junktionen aneinander und an die innere Oberfläche der Dura mater geschaltet, und sie bilden einen Teil der Blut – Liquor bzw. der Hirn – Liquor Schranke.
Die Deckzellen befinden sich an der äusseren Oberfläche der Arachnoidea, und bedecken auch den Plexus choroideus. Der mit Liquor (auf englisch CSF – cerebro-spinal fluid) ausgefüllte Subarachnoidalraum wird durch feine Fasern der Arachnoidea überbrückt , die auch trabekuläre arachnoidale Zellen genannt werden. Die Ultrastruktur dieser Zellen und die EMA (epitheliales Membran Antigen) Positivität deuten auf den epithelialen Ursprung dieser Zellen hin. Sie haben aber auch einen mesenchymalen Charakter, da sie zur Kollagensynthese und zur Synthese anderer stromaler Proteine fähig sind, und oft an Fibroblasten erinnern. Diese Zellen sind auch stark Vimentin positiv, und auf pathologische Reize reagieren sie mit der Bildung einer Fibrose.
VII./2.3.2.2.: Funktionelle Eigenschaften
|
| |
Diese Zellen spielen eine wichtige Rolle bei der Regulation des intrakraniellen Druckes (ic), bei der Aufrechterhaltung der CSF – der Homeostase bzw. dem Ableiten des CSF, da die arachnoidealen Villi eine Art Ventil zwischen dem Liquorraum und dem Blut der Venen – venösen Sinuse bilden. Sie sind auch zur Sekretion fähig, was den epithelialen Charakter dieser Zellen unterstreicht (ausserdem, dass sie ja auch zur Bildung von Desmosomen und anderen Junktionen fähig sind); sie sezernieren Liquorproteine (IGF-II, IGFBP-II, apo-E,beta2-Mikroglobulin) und Enzyme (Prostaglandin D-Synthase), glioneurale – und Proliferationsfaktoren. Bilden diese Zellen Tumore, so zeigt sich oft eine Hyperostose, die damit erklärt wird, dass diese Zellen zur Sekretion von alkalischer Phosphatase fähig sind. Ausserdem sind diese Zell bei der Auswahl der Chemokine mit beteiligt, die mit zur Bildung des Stratum granulosum externum der Kleinhirnrinde beitragen; sie sind ausserdem noch zur Bildung von glialen und neurotrophischen Zytokinen fähig.
VII./2.3.2.3.: Pathologische Zustände der meningothelialen Zellen
|
 |
Der epitheliale Charakter der Zellen zeigt sich besonders bei den sog.sekretorischen Meningeomen. Bei solchen Tumoren sieht man oft eine glanduläre Metaplasie und eine intrazytoplasmatische Lumenbildung, und ausserdem bilden sich Mikrovilli und Zilien an der Zelloberfläche. Das sekretierte Material ist ein Eiweiss und wird als Pseudo-Psammomkörper bezeichnet. Diese Zellen sind oft Zytokeratin und CEA-positiv.
Falls es nötig ist, können diese Zellen auch als Monozyten/Makrophagen funktionieren. Ausserdem können sie an der Bildung von Fremdkörper –Riesenzellen oder rheumatischen Noduli beteiligt sein, oder sich lympho-plasmozytäre Strukturen einverleiben (Emperipolesis) bzw.bei der HLA- Expression beteiligt sein.
Auf pathologische Reize reagieren sie mit einer reaktiven Hyperplasie, bei extremen Noxen können sich auch Tumore bilden. Die meningeale Hyperplasie ist meist multifokal, betrifft mehr als 10 Zellschichten und kommt oft nach einer Blutung, einer Entzündung, wegen einer mechanischen/chemischen Irritation, oder wegen Traumen zustande. Paradoxer Weise kann es sogar sein, dass sich solch eine Hyperplasie durch einen Tumor bildet: es ist ein Fall dokumentiert worden, wo sich durch die mechanische Irritation eines Glioms, das bis an die arachnoidale Oberfläche gewachsen ist, sekundär ein sarkomatöses Meningeom gebildet hat (Sarkogliom).
Die Liste der Funktion dieser Zellen ist noch längst nicht vollständig, da viele ihrer Eigenschaften bis zum heutigen Tag nicht eindeutig geklärt sind. Zur Erforschung dieser Zellen hat János Kepes, ein in den USA arbeitender Neuropathologe ungarischer Herkunft , beigetragen. Die breite Skala der Funktion erklärt, warum sich so viele Arten von Tumoren (Meningeomata) aus dieser Zellart bilden können.
VII./2.3.3.: Typische Lokalisation der Meningeome
|
| |
Die meisten Meningeome sind intrakranial oder intraspinal lokalisiert. Intrakranial befinden sich Meningeome meist an der Konvexität der Hemisphäre(1.Makrofoto), in der Falx cerebri (2.Makrofoto), im Sulcus olfactorius, an den Rändern ders Os sphenoidale (3.Makrofoto), in der Gegend der Sella turcica, in der Pars petrosa des Ossis temporalis, am Rand des Tentorium cerebelli, oder in der hinteren Schädelgrube. Die Meningeome der Tela choroidea, die intraventrikulären, oder die Meningeome des Plexus choroideus, die eine bisher ungeklärte Prädilektionsstelle im linken Ventrikel aufzeigen, sind um einiges seltener.
|

Beurteilen Sie das Bild!
|
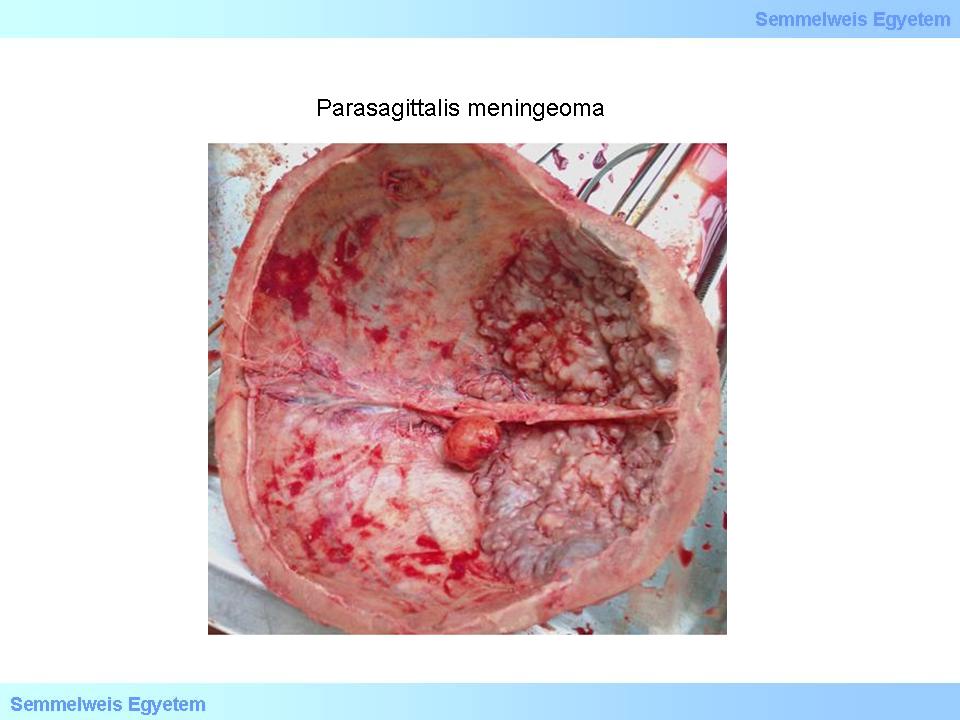
1.Makrofoto:Parasaggitales Meningeom, dass sich in den interhemisphäralen Sulcus eingebettet hat. Solche Tumore verursachen verständlicher Weise oft epileptische Anfälle und Kopfschmerzen.
|

2.Makrofoto: Parasaggitales Meningeom (Falx cerebri). Der Tumor hat wirklich ein tumorartiges Aussehen (knotenartig), und eine relativ glatte Oberfläche. Die starke frontale Hyperostose stellt eine vom Tumor unabhängige Veränderung dar.
|
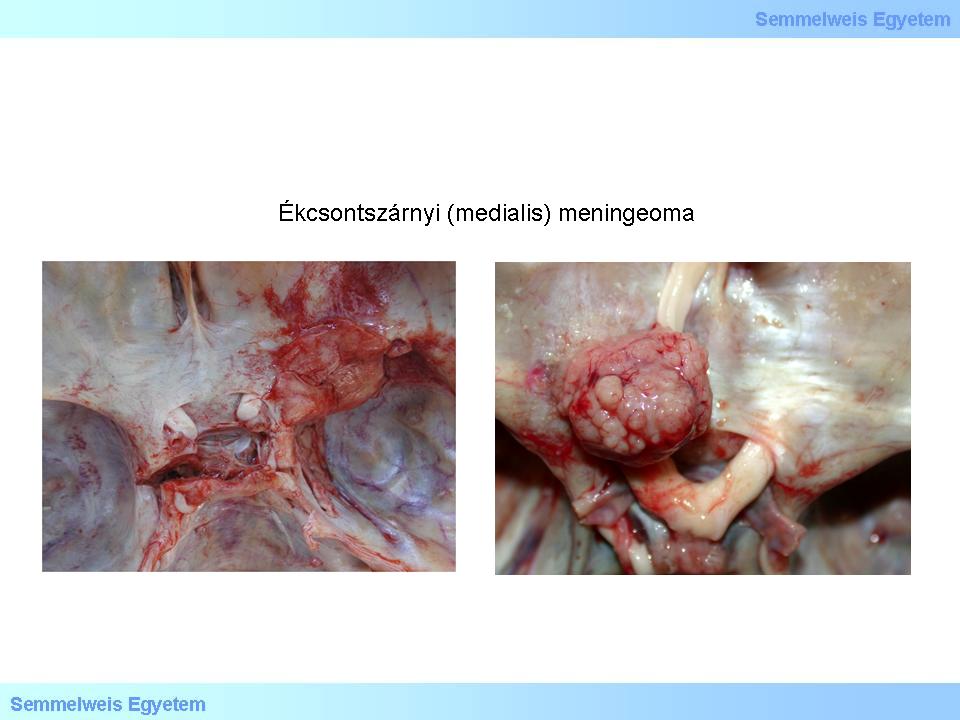
3A-B. Makrofoto: Meningeom des Os sphenoidale (medial). Die Oberfläche des Tumors scheint manchmal schleimig glänzend, manchmal ist sie aber auch knotig und unregelmässig. Die radikale operative Entfernung eines Meningeoms der Hirnbasis ist aus technischen Gründen oft nicht ausführbar
|
Spinale Meningeome bilden sich meist im thorakalen Rückenmark, die Meningeome des cervikalen oder des lumbalen Rückenmarkes wiederum sind sehr selten. Die ausserhalb des Kranio- Spinalen Areals vorkommenden Meningeome sind zervikal lokalisiert, oder sie kommen in der Orbita (Sehnenscheide des N.Optikus), glabellar, sinonasal, oropharyngeal, subgaleal, juxtaparotidal, oder kutan vor. In ganz besonders seltenen Fällen kommen Meningeome auch noch weiter von der zentralen Neuroaxis entfernt, so z.B. im Mediastinum, in den Lungen, oder im Plexus brachialis, vor.
VII./2.3.4.: Die Wirkung von Hormonen auf meningeale Tumore
|
 |
Diese Frage beschäftigt die Neuro-Onkopathologen schon seit langem. Die weibliche Dominanz der Meningeome im Verhältnis 2:1 ist seit langem bekannt, die bei thorakal/ spinal lokalisierten Tumoren sogar ein Verhältnis von 9:1 annehmen kann. Ausserdem fangen diese Tumore bei einer eventuellen Schwangerschaft meist ganz extrem an zu wachsen, was sich in erster Linie auf Meningeome am Nervus opticus auswirkt und sich so Symptome verstärken, die mit der Kompression des N.opticus in zusammenhang zu bringen sind; nach Ablauf der der Schwangerschaft (post partum) bessern sich die Symptome, bei einer erneuten Schwangerschaft treten die Symptome aber wieder auf . Diese sich bei einer Schwangerschaft ergebende Verschlechterung der Symptome eines Meningeoms wird auf die vaskuläre Congestion und das zytotoxische Ödem zurückgeführt, da sich die Mitotische Aktivität des Tumors bei dieset Art des Wachstums nicht erhöht.
Bei 50-80% der Meningeome kann ein Progesteronrezeptor (PR) nachgewiesen werden. Dies wird mit dem entsprechenden Antikörper aufgezeigt, der im Zellkern stark positiv ist; diese Reaktion ist für Östrogen Rezeptoren eigentlich negativ, was heisst, dass Östrogen Rezeptoren kaum expressiert werden. Die Intensität der PR-Expression ist oft anti-proportional zum Grad des Tumors, die folglich bei anaplastischen und malignen Melanomen gänzlich fehlt. Die Rolle des PRs ist immernoch nicht ganz geklärt, für eine Hormonabhängigkeit des Tumors spricht aber die Tatsache, dass das Risiko für die Bildung eines Meningeoms bei der Einnahme von oralen Antikonzipienten und nach einer Hormontherapie erhöht ist, und Meningeome sich auch oft parallel zu den ebenfalls Hormon abhängigen Brustkarzinomen ausbilden. Trotzdem kann man auch oft eine PR-Expression bei Meningeomen von Männern und Kindern sehen.
VII./2.3.5.: Zytogenetischer und molekulargenetischer Hintergrund der Meningeome
Es gibt einige Chromosomenfehler, die massgeblich für die meningealen Tumore sind, wobei es sich in erster Linie um Chromosomenverluste handelt, die zur Hypoploidität führen. Hierbei kommen die Monosomie 22, die partiale Deletion des 22q, bzw. die Verluste des 6., des 10., des 14. und des 18. Chromosomes häufig vor. Die 22q Deletion kann mit einer FISH bzw. einer LOH –Untersuchung (loss of heterozigosity) nachgewiesen werden; ferner kann so bewiesen werden, dass weitere zytogenetische und molekulargenetische Abnormitäten hinzu kommen müssen, dass der Tumor von einem WHO Gr I. bis zu einem Gr III. mutiert. Diese konsekutive Folgerung ist aber nicht verpflichtend und linear.
Die Tatsache, dass es bei der Bildung eines Meningeoms zum Chromosomenverlust kommen muss, lässt darauf schliessen, dass es spezifische Suppressorgene gibt. Untersuchungen zum 22q Verlust haben dies am eindeutigsten aufgezeigt. Das NF2-Gen sitzt auf dem Lokus 22q12.2 und synthetisiert ein Eiweiss, das Merlin genannt wird. Die Tumore, die am 2. häufigsten wegen einer 22q Deletion zustande kommen, sind die Meningeome (an erster Stelle stehen die Schwannome). Die NF2 –assoziierten Meningeome sind oft multipel, und es ist leicht verständlich, dass sie zusammen mit einer Neurofibromatose (NF-2) vorkommen.
Dem heutigen Stand der Wissenschaft nach geht man davon aus, dass das NF2 –Gen für die Bildung der Meningeome, und nicht für ihre Progression verantwortlich ist. Eine sporadische NF2 –Genmutation ist beim fibrösen und transitionalzellulären Typ der Meningeome besonders häufig (s.unten). Interessant ist ferner, dass dieser Prozentsatz bei meningothelialen Meningeomen auf 25% sinkt, und dort am ehesten die an der Hirnbasis lokalisierten Tumore betrifft. Diese Tatsache lässt auch darauf schliessen, dass es auch noch andere Arten, nicht nur den NF2 assoziierten Weg der Tumorbildung, gibt . Wird ein Meningeom bei Kindern oder Jugendlichen diagnostisiert, muss immer an eine noch nicht manifeste NF-2 gedacht werden, und es müssen Untersuchungen in dieser Richtung veranlasst werden. Welche Gene für die Progression eines Meningeoms verantwortlich gemacht werden können, ist noch nicht eindeutig geklärt. Es muss hier allerdings noch erwähnt werden, dass ein Verlust der CDKN2A/p16 – Region (9p21-er Lokus) bei anaplastischen Meningeomen eine schlechte Prognose bedeutet; die Untersuchung des 9p21 mit einer FISH kann also prognostischen Wert haben!
VII./2.3.6.: Kliniko – pathologischer Hintergrund und biologisches Potential der Meningeome
|
 |
Meningeome gehen also von den Meningen aus, wachsen i. A. langsam, sind mit der Dura verbunden, und kommen meist im Erwachsenenalter, manchmal aber auch im Kindes- oder Jugendlichenalter vor, und zeigen eine weibliche dominanz. Ionisierende Strahlen in der Kopfregion erhöhen laut mehrerer voneinander unabhängiger epidemiologischer Angaben das Risiko für die Bildung solch eines Tumors. Die Tumore, die sich nach einer Bestrahlung bilden, sind oft multipel, vom histologischen Phänotyp her eher atypisch, und klinisch agressiver. Es gibt sowohl benigne als auch maligne Formen. Aus neuroradiologischer Sicht ist ein typisches Meningeom solide, rund oder lamelliert, und bildet eine Tumormasse, die bis an die Dura reicht.
Es kann auch sein, dass der Tumor nicht rund ist, sondern die Ursprungsstelle Schichten weise bedeckt: Meningeoma en plaque. Dieser Tumor wächst verdrängend, und breitet sich nicht selten bis an die Dura mater, bzw. an die angrenzenden Sinuse aus. Es kommt auch vor, dass der Tumor sich auf den Schädelknochen ausbreitet, oder ihn auch durchbricht, und an der äusseren Konvexität des Schädels als subaponeurotisch-subkutanes Gebilde erscheint. Dieses makroskopische Verhalten bedeutet nicht unbedingt, dass der Tumor ein biologisch agressives Potenzial hat (sog. Malignität).
Klinisch muss ausserdem noch beachtet werden, dass dieser Tumor ein ausgesprochen hohes Potential zur Rezidivbildung zeigt. Ferner hängt die Rezidivbildung der einzelnen Meningeomtypen von der Radikalität der chirurgischen Entfernung ab, die wiederum grundsätzlich von der Lokalisation des Tumors abhängig gemacht werden muss (20P-3.Makrofoto). Auch bei Tumoren, die als restlos entfernt (in toto) gelten, können Rezidive vorkommen; der genaue molekulargenetische Hintergrund dieses Vorganges ist noch nicht geklärt. Die Infiltration der Dura mater ist eigentlich bei jedem Meningeom zu beobachten (4.Makrofoto). Die Invasion des Gehirnparenchyms bedeutet nicht unbedingt, dass der Tumor maligne ist; neueste Studien haben aber gezeigt, dass solche Tumore („brain invasive meningeoma”) von ihrer histologischen Struktur unabhängig laut WHO als Gr II. Tumore eingeordnet werden müssen, und Patienten mit solch einem Tumor längere Zeit lang kontrolliert werden müssen, da die Invasion des Gehirnparenchyms als Zeichen der klinischen Agressivität gilt.
|

Beurteilen Sie das Bild!
|
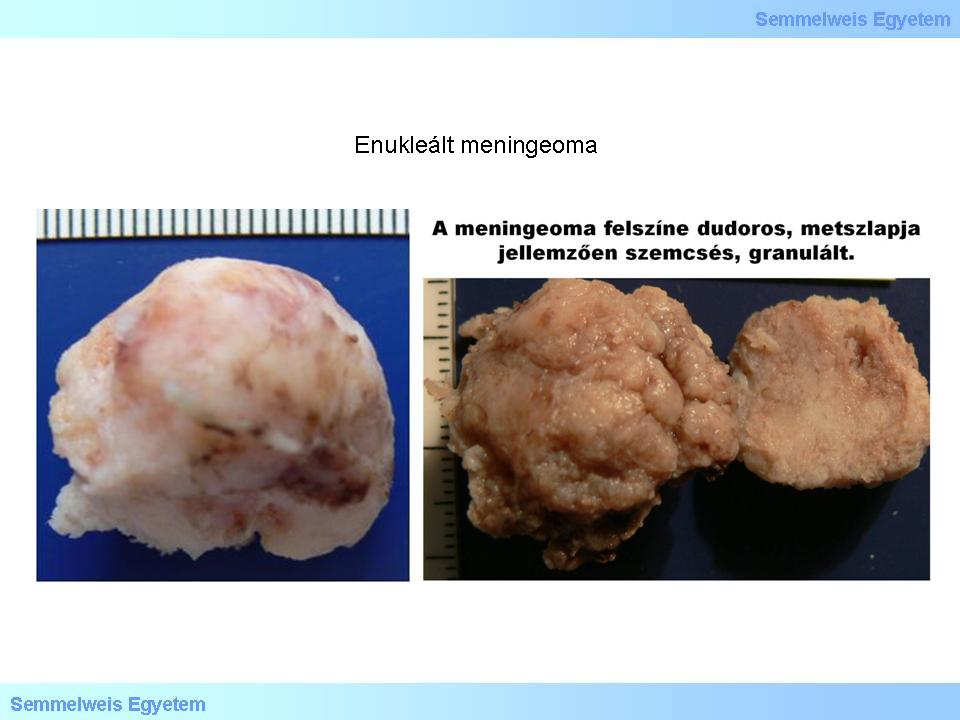
4A-B.Makrofoto: Enukleirtes Meningeom. Der Tumor ist knotenartig, hat einen unregelmässigen Rand und eine ebenfalls knotige Oberfläche, und ist dabei doch glatt (was als paradox erscheint); die Schnittfläche des Tumors ist fein granuliert. Es sind Einblutungen in Form von bräunlich-roten Arealen zu sehen.
|
Die meisten Meningeome erscheinen auf einem CT oder einem T1-MR Aufnahme mehr isodens als der Cortex, was die genaue Beurteilung ihrer Grösse erschwert. Das „dural tail” – Zeichen kann nach der Gabe von Kontrastmitteln gesehen werden, und bedeutet, dass der Tumor wirklich extraaxial lokalisiert ist. Tumore höheren Grades können neuroradiologisch gut identifiziert werden, da sie sowohl auf den T1 als auch auf den T2 –MR Aufnahmen intensiver erscheinen, die Tumorgrenzen verwaschen sind, sich das sog. „mushrooming” zeigt (multiples noduläres Gebilde, dass sich ins Gehirnparenchym „reindrückt”), dieser Tumor auf T1 Aufnahmen dunkel, auf T2 Aufnahmen hell erscheint, und sich Flecken innerhalb des Tumors zeigen (Tumornekrosen).
VII./2.3.7.: Makroskopische Erscheinung
Die makroskopische Erscheinung der Meningeome ist sehr unterschiedlich, sie sind oft nodulär oder sogar Kartoffel artig, sie können aber auch ganz dünne Platten bilden, die sich an die Dura mater anschmiegen (s. die sog. en plaque Tumore). Die Tumore sind meist gut umschrieben (demarkiert), haben eine feste Konsistenz, und sind Gummi artig oder hart, bzw. können eine Sand artige Konsistenz („gritty”) haben, was dann mit einer Kalzifikation oder dem Vorhandensein unendlich vieler Psammomkörper zusammen vorkommt (5.Makrofoto). Es ist verständlich, dass es sehr schwer ist, aus solch einem Tumor einen Abstrich/Gefrierpräparat, geschweige denn ein in Paraffin eingebettetes Präparat zu gewinnen. Die nekrotischen und eingebluteten Tumorknoten haben eine weiche Konsistenz, eine Gelee artige Konsistenz ist sehr selten, und kommt meist durch eine adenomatoide Metaplasie zustande.
|

Beurteilen Sie das Bild!
|
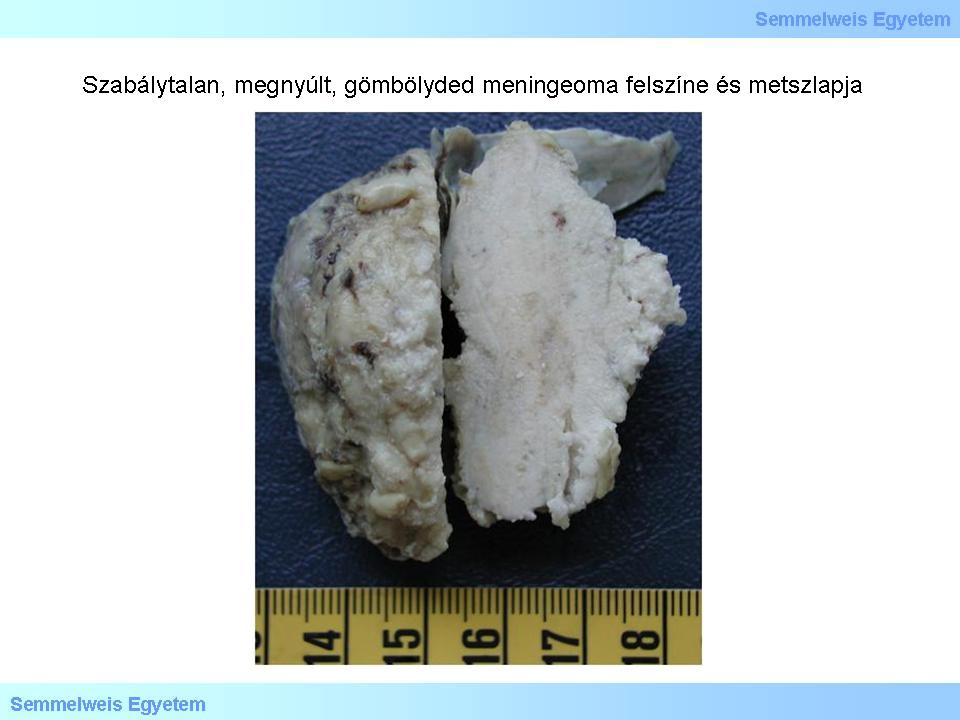
5.Makrofoto: Oberfläche und Schnittfläche eines unregelmässigen, länglichen, aber doch runden Meningeoms. Die Oberfläche ist knotig, mikronodulär, die Schnittfläche ist unregelmässig, wie Schleifpapier („gritty), was auf das Vorhandensein extrem vieler Psammomkörper hindeutet. Der Teil des Tumors, der mit der Dura mater verbunden ist, und der auf radiologischen Aufnahmen sichtbare „durale Schwanz” (dural tail) ist gut zu sehen.
|
Die Schnittfläche dieser Tumore ist mehr oder weniger homogen, und enthält oft Spiral artige Fasern (ähnlich wie bei Leiomyomen). Die dominierende Färbung der Tumore ist gräulich-weiss, sie können aber auch schwarz-rote Areale (Blutungen), und gelbliche Flecken (erhöhter Lipidgehalt: xanthomatöse Transformation, fettzellige Metaplasie) enthalten. Die Areale, die eine Knochen- oder Knorpelmetaplasie enthalten, sind weiss. In den komprimierten, angrenzenden Hirnarealen kommt es oft zu kleinen Blutungen.
Die Meningeome vom „klassischen” histologischen Typ (s.unten) sind oft unterhalb des Lobus frontalis, in der Olfaktorius Region lokalisiert (subfrontales Meningeom). Der oft - im Gegensatz dazu wie wenig Raum es im Schädel gibt - sehr gross wachsende Tumor verschiebt das Frontalhirn, und mit ihm auch oft den Hypothalamus, nach oben. Der Tumor kann sogar so gross werden, dass er die Ventrikel komprimiert. Die Folge dieser Kompression ist dann oft, dass das Verhalten, das Denken und der Intellekt der Patienten sich immer mehr und mehr abbaut oder verändert. Diese Veränderung der Charaktere geht auch relativ häufig in eine Agressivität über, der Patient wird paranoid, und bekommt oft Wutanfälle, in denen er mit obszönen Ausdrücken um sich schmeisst, weshalb diese Patienten oft in der Psychiatrie enden; denkt auch das Pflegepersonal in der Psychatrie nicht daran, dass der Auslöser der Symptome bei solch einem Patienten nicht nur eine aspezifische Demenz sein könnte, wird das Meningeom oft nur bei einer Sektion entdeckt.
VII./2.3.8.: Histologie der Meningeome
VII./2.3.8.1.: Allgemeine Eigenschaften
|
 |
Am häufigsten bilden sich Gr I. Tumore aus, die also vom Zellaufbau und ihrem biologischen Verhalten her benigne sind; einige histologische Untertypen haben allerdings eine schlechtere Prognose und einen ungünstigeren klinischen Verlauf, und werden somit als Gr II. oder Gr III. eingeteilt. Falls der Proliferationsindex solch eines Tumors hoch ist, hat er ein hohes Potential zur Bildung von Rezidiven, zeigt ein agressives Verhalten, und /oder wächst invasiv ins Gehirnparenchym. Aber das histologische Bild ist nicht immer ausschlaggebend für die Aufstellung der Prognose eines Meningeoms. Dazu benutzt man die Bestimmung des Proliferationsindex, der immunhistochemisch (IHC) mit den Ki67 (MIB-1) benannten monoklonalen Antikörpern geschieht.
An dieser Stelle muss allerdings bemerkt werden, dass der mit immunhistochemischen Methoden bestimmte Mib-1 (Ki-67) Index (auf engl.: LI – labelling index) viel weniger mit dem biologischen Verhalten korreliert, als wenn man an einem HE –gefärbten Präparat de facto die Zahl der Mitosen bestimmen würde. Kann man in einem Meningeom, unabhängig von dessen Differenzierungsgrad, mehr als 20 Mitosen /10 SGV sieht, kann der Tumor sicher als maligne Eingestuft werden (SGV – Sichtfeld grosser Vergrösserung; engl. HPF – high power field; 40x –es Objektiv, d.h. mit einer 400x fachen Vergrösserung pro Sichtfeld). Es ist also noch nicht definiert, ob allein anhand des Mib-1 Index eine unabhängige Prognose aufgestellt werden kann, da die Intensität der IHC –en Methoden subjektiv bewertet werden müssen, was von Labor zu Labor ja unterschiedlich ist.
VII./2.3.8.2.: Bestimmung des histologischen Grades
Die WHO Einteilung (2007) unterscheidet 16 verschiedene Typen/ Varianten dieses Tumors, die in 3 verschiedene Grade eingeteilt werden können (Tabelle 1).
|

Beurteilen Sie die Tabelle!
|
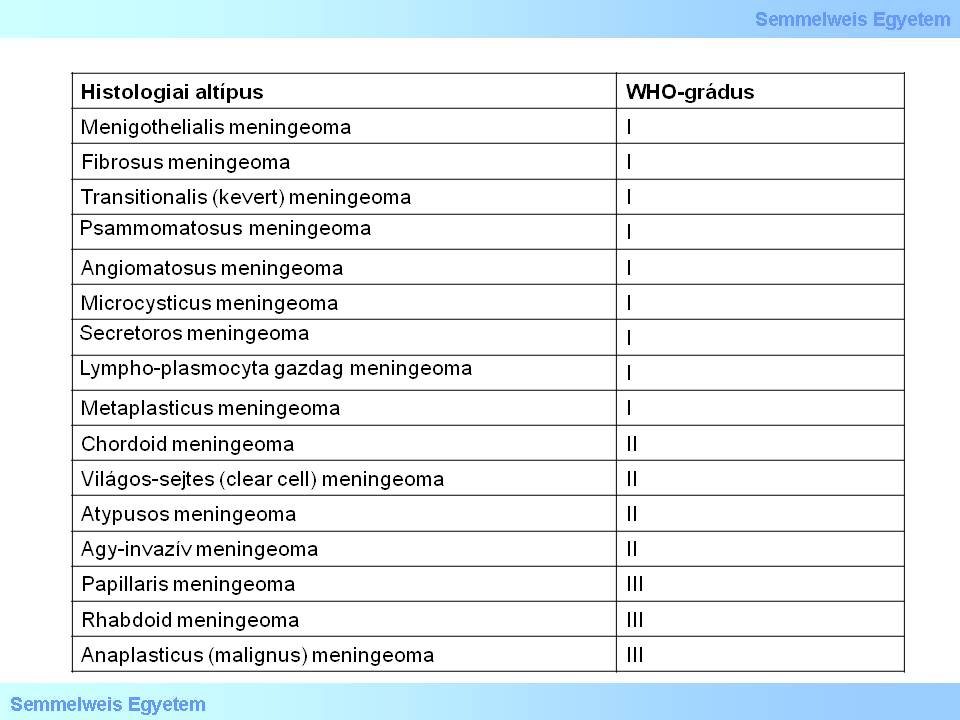
Tabelle 1: Histologische Betimmung des Tumor Grades.
|
VII./2.3.8.3.: „Klassische” Typen der Meningeome
Der am häufigsten vorkommende „klassische” Typ der Meningeome ist das meningotheliale Meningeom. Für diesen Typ ist es spezifisch, dass die tumorösen arachnoidealen Zellen unregelmässige, Mosaik artige Nester bilden, die sich locker aneinander reihen. Das Bild ist monomorph, und man sieht spezifische Zellkerne. Es kommt nicht selten vor, dass auch eine regressive Verfettung zu beobachten ist (sog. Lipidisation, xanthomatöse Transformation) oder sich im Zentrum des Tumors eine schleimige Degeneration bildet. Ausserdem sieht man in einem meningothelialen Meningeom im Zellkern kleine helle intranukleare Einschlusskörper (Pseudoinklusion), von denen man manchmal ganz extrem viele sehen kann, was bei der Differentialdiagnose dieses Tumors nützlich sein kann. Weiterhin typisch für diese Meningeome ist, dass sie sich um meningotheliale Lobuli, um dünne fibröse Septen herum anordnen. Ganz verstreut kann der eine oder andere Psammomkörper vorkommen; bei meningothelialen Meningeomen ist die Zahl Letzterer niedrig, es gibt aber viele Meningeome, die voll von Psammomkörpern sind, und dann dem entsprechend als psammomatöse Form bezeichnet werden.
Die andere „klassische” Form der Meningeome sind die fibrösen Meningeome = meningeoma fibrosum (oder auch fibroblastär, was aber nicht korrekt ist, weil es sich bei diesen Zellen um meningotheliale Elemente, und nicht um Fibroblasten handelt). Histologisch sieht man parallel verlaufende, Spindel- oder Zigarren förmige Zellbündel (die übrigens wirklich an Fibroblasten erinnern), die mässig hyperchrome Zellkerne haben. Diese Bündel überkreuzen sich von Zeit zu Zeit und bilden so eine Netz artige Struktur, in die Massen von Kollagen und retikulären Fasern eingearbeitet sind; die Menge an Kollagen kann ganz beträchtliche Masse annehmen.
VII./2.3.8.4.: Weitere histologische Varianten
|
 |
Das transitionale Meningeom ist eine Mischung aus dem meningotheliomatösen und dem fibrösen Typ. Das mikrozystische Meningeom hat typischer Weise viele dünne Tumorausläufer, die dem Tumor das Aussehen eines „löchrigen” Netzes verleihen. Das Lymphoplasmozyten reiche Meningeom kann so viele chronische Entzündungszellen beinhalten, dass man es oft differentialdiagnostisch nicht von einer Entzündung unterscheiden kann. Das chordoide Meningeom erinnert, wie der Name schon sagt, an ein Chordom notochordalen Ursprunges. Ein metaplastisches Meningeom enthält Knochen, Knorpel und Fettgewebe. Das lipomatöse Meningeom entsteht wahrscheinlich nicht durch eine echte Metaplasie, sondern durch eine progressive xanthomatöse Veränderung und eine unspezifische Verfettung.
Sklerosierende Meningeome werden in der WHO Einteilung nicht erwähnt, es gibt sie aber trotzdem. Typisch für dieses Meningeom sind Massen von einem hyalinär veränderten amanthoiden Kollagen. Diese verdickten Fasern bilden oft Knoten artige Gebilde von mehreren Mikrometern Durchmesser. In der WHO Einteilung fehlt ebenfalls das onkozytäre Meningeom und das myxoide/ muzinöse Meningeom. Letzteres entspricht den chordoiden und myxoid- metaplastischen Meningeomen. Das hellzellige (clear-cell) Meningeom, das rhabdoide Meningeom (1.Mikrofoto) und das papilläre Meningeom gehören einem höheren Grad an (s.unten). Die Kriterien des atypischen Meningeoms haben Arie Perry und Mitarbeiter geklärt, die die WHO dann im Jahr 2000 übernommen hat, und im Jahr 2007 nochmals verändert hat. Das anaplastische Meningeom (Meningeoma malignum) ist ähnlich wie ein Fibrosarkom, zeigt auch Elemente eines anaplastischen Karzinoms, und erinnert auch an ein Melanom.
|

Beurteilen Sie das Bild!
|

1.Mikrofoto: Rhabdoides Meningeom. Laut Definition handelt es sich um einen Tumor hohen Grades.
|
VII./2.3.8.5.: WHO –Kriterien zur Bestimmung des Tumorgrades
Die Meningeome sind eines der am meisten umstrittenen Gebiete der Neuro-Onkopathologie. Die WHO teilt 4 Untertypen der Meningeome höheren Grades ein:
-
1. die „clear cell” Meningeome (Gr.II.),
-
2. die chordoiden Meningeome (Gr. II.),
-
3. das rhabdoide Meningeom (Gr.III.) und
-
4. das papilläre Meningeom (Gr.III.).
Die Frage, wie gross das betroffene tumoröse Areal dazu sein muss, dass es die Einteilung in einen Tumor höheren Grades bekommt, ist bis zum heutigen Tag ungeklärt
VII./2.3.8.5.1.: Benignus meningeoma (WHO GrI.)
Hierzu gehört jegliche dominierende histologische Art des Meningeoms, ausser der chordoiden, der clear cell Typ, der papillären oder rhabdoiden Form der Meningeome. Die Kriterien für die atypischen, die invasiv ins Gehirnparenchym infiltrierenden und für die anaplastischen Meningeome fehlen.
VII./2.3.8.5.2.: Atypische Meningeome (WHO Gr II.)
(20P-2.Mikrofoto). Eine erhöhte Mitoserate : mehr als 4 Mitosen / 10 SGV. Wichtig: das bezieht sich nicht auf das Ergebnis der Ki-67 IHC – Reaktion! Ausserdem müssen mindestens 3 der 5 folgenden Kriterien erfüllt werden:
-
1. „sheeting” (sheet – Tuch) – sich wie ein breites Feld verteilender Tumor ohne wirkliche Struktur, und ohne Strudel, Nester, Septen, Lobuli, usw.;
-
2. kleinzellige Metaplasie, d.h. Lymphozyten artige Tumorzellen mit grossen Zellkernen (das Verhältnis des Kernes zum Zytoplasma ist zugunsten des Kernes verschoben (N/C);
-
3. Hyperzellularität
-
4. auffällig grosse, prominente sog. „Makronukleoli”;
-
5. spontane Nekrosen (Zellabsterben, dass nicht wegen einer Embolisation oder einer Strahlentherapie zustande gekommen ist; es handelt sich um eine sui generis Tumornekrose).
|

Beurteilen Sie das Bild!
|
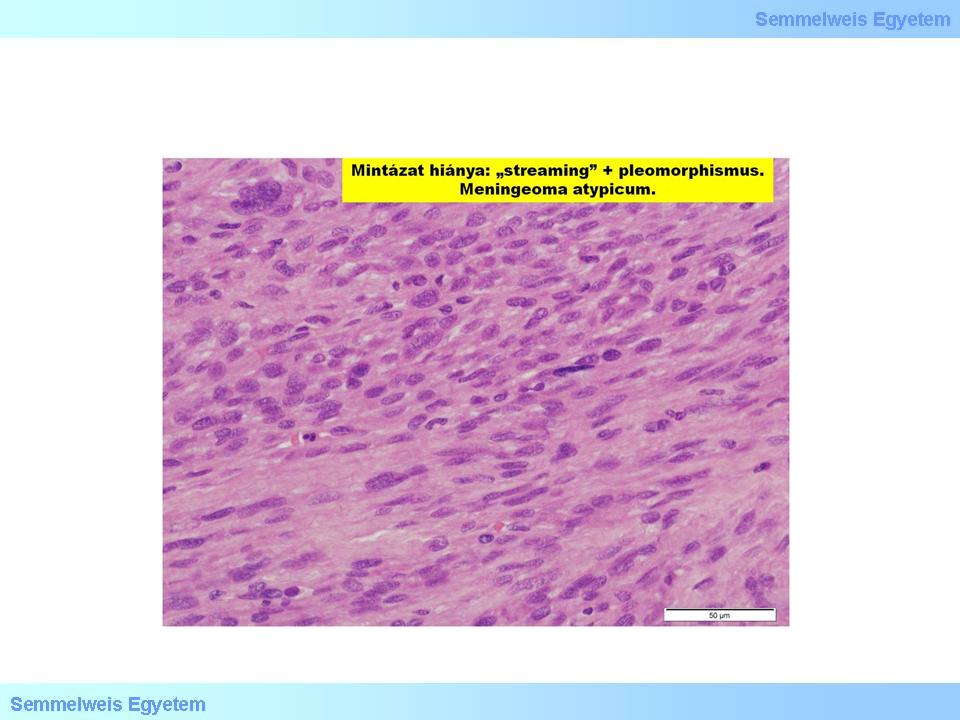
2.Mikrofoto: Atypisches Meningeom. Es fehlt eine wirkliche Struktur (sheeting), und es ist ein Pleomorphismus zu sehen.
|
VII./2.3.8.5.3. Invasiv ins Gehirnparenchym wachsender Tumor (WHO Gr II.)
Das tumoröse meningeale Gewebe wächst mit Zungen artigen Ausläufern in das Gehirn ein. Die relativ scharfe Grenze der Protrusionen kann irreführend sein. Im Meningeom selber sind GFAP – positive Inseln aus Neuropil detektierbar („incorporatio”).
VII./2.3.8.5.4.: Anaplastische (maligne) Meningeome (WHO Gr III.).)
Von den folgenden 2 Kriterien muss mindestens eines vorhanden sein:
-
- die Mitoserate muss bei über 20 Mitosen/10 SGV liegen.
-
- eindeutige Anaplasie (eine Sarkom- , Karzinom-, oder Melanom artige Zytologie /Histologie).
Die bisher beschriebene Einteilung beruht auf viele subjektive Kriterien (z.B. „sheeting”, kleinzellige Varianten, usw.), dieses System wird aber weltweit akzeptiert und angewandt. Die nächste WHO – Einteilung der Meningeome wird wahrscheinlich viel mehr molekuläre / genetische Kriterien in Betracht ziehen
|
|