| |
XIII./4. fejezet: Klinikai példák a genomikai markerek felhasználására
XIII./4.1. Prevenciós orvoslás
A mai mindennapi klinikai gyakorlatban már tudunk számos példát hozni. A monogénes betegségekben a betegség megelőzése a fontos szempont. Abban az esetben, ha a preszimptómás állapotban már ismerjük, hogy valaki hordozza vagy nem a betegséget kiváltó genetikai hibát, a prenatális diagnosztikával a következő generációban megelőzhető a betegség. Pl. tudjuk, hogy a spinalis izomatrophia oka az SMN gén deléciója a kaukázusi populációban nagyon gyakori, azaz sokan hordozzuk a mutációt, anélkül, hogy betegek lennénk. Mivel az autosomalis recesszív spinalis izomatrophia már csecsemőkorban gyakran halált okoz, azon családok tagjai ahol a betegség korábban már előfordult egyre gyakrabban a családtervezéskor már kérik genetikai vizsgálatukat, hogy megelőzzék a betegséget.
|
A tudtad, hogy Angelina Jolie emlőit és petefészkeit is azért távolították el, mert családjában halmozódtak ezek a tumorok és a BRCAa/2 génjeiben magas rizikójú variánsokat találta? Angelina úgy döntött megelőzi az emlőrákot.
|
Az örökletes tumor syndromáknál a betegségre hajlamosító genetikai-genomikai rizikótényezőket keressük. Pl. BRCA1/2 gének mutációjának jelenléte az emlő és petefészek rák rizikóját nagymértékben emeli, így a preszimptómás állapotban egy ilyen rizikófaktornak az ismerete lehetővé teszi a beteg számára, hogy pozitív családi anamnézis mellett már a betegség kialakulása előtt tegyen annak érdekében, hogy ne alakuljon ki a klinikai tünet (7. Ábra). Lehetőség van pl. emlő ablációra az emlőrák kialakulása előtt.
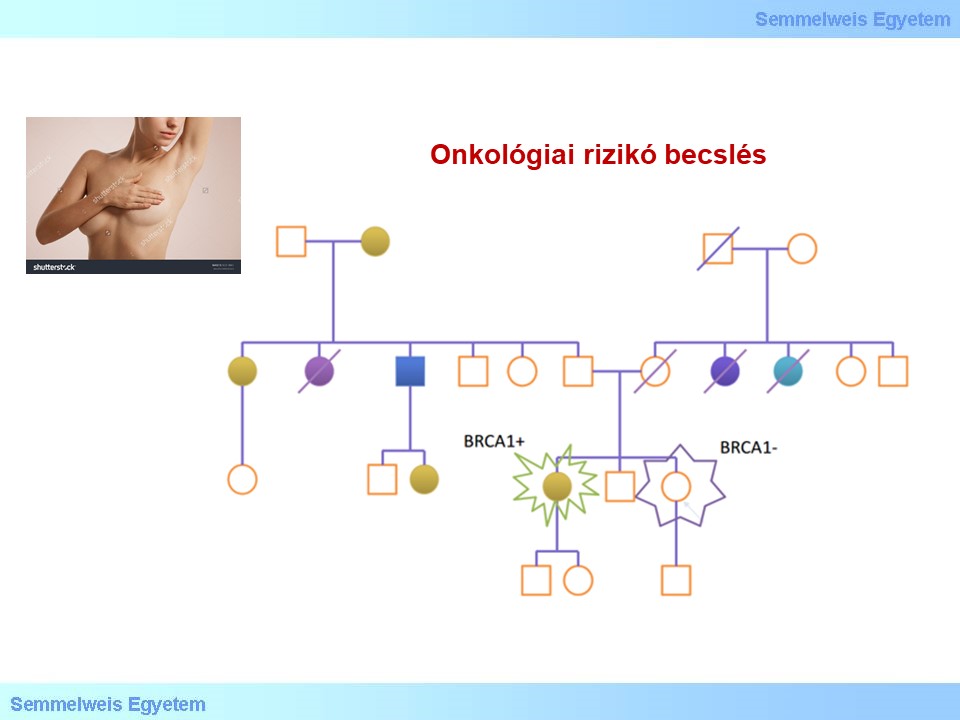
7. ábra: Onkológiai rizikóbecslés
|
XIII./4.2. Betegség menedzsment
Monogénes betegségek: a fentiekben említett spinalis izomatrophiában már rendelkezünk mutáció specifikus kezelési lehetőséggel. Azoknak a pácienseknek, akiknek az SMN1 génjének a deléciója okozza a betegséget és az SMN2 génjüknek legalább 2 kópiája van egy olyan mRNS splicingot módosító kezelést tudunk kínálni, mely segítségével javul az SMN2-ról átíródó fehérje expressziója és ezáltal enyhülnek a klinikai tünetek.

8. ábra
|
Mutáció specifikus terápiát tudunk kínálni a Duchenne typusú izomdystrophiában. Egyes eseteiben a betegség a dystrophin gén korai stop mutációja miatt alakul ki, van egy olyan gyógyszer, ami a kóros stop mutációt el tudja maszkírozni és a transzláció nem áll le ennél a lépésnél, hanem a sejt átugorja a hibás stop kodont és normalizálódik a transzláció. Természetesen ez a gyógyszer csak olyan Duchennes kisfiúknak tud segíteni, akiknek ez a típusú hiba okozza a panaszait. Az összes Duchennes beteg kb. 13% ban okozza a korai stop kodon mutáció a betegséget.

9. ábra
|
|

A modern onkológiai kezelések alapját képezik a molekuláris patológiai vizsgálatok. A tumorok expressziós mintázatának ismerete segíti az onkológust a terápia kiválasztásában.
|
A fenotípus alapján sok esetben nincs lehetőségünk a pontos etiológiát megállapítani. Pl. korai kezdetű Parkinson kór esetén a betegséget okozhatja monogénes betegség pl. parkin mutáció, PINK1, DJ1 gén mutációja, de lehetnek a tünetek polygénes, komplex betegség következményei, sőt esetenként encephalitis következményeként alakul ki a betegség (pl. Economo encephalitis). Ilyen esetben a genetikai diagnosztika nagyon fontos a pontos diagnózis és a betegség stratifikáció szempontjából. A parkin mutáció következtében kialakuló betegségben nagyon jó a levadopa válasz, így hiába fiatal a beteg nem a dopamin antagonistákkal kezdjük a kezelés, hanem korán bevetjük a levadopa készítményeket.
A polygénes, komplex multifaktoriális betegségekben, pl. az emlő tumorban bizonyos fehérjéknek az expressziója (pl. HER2) lehetővé teszi olyan gyógyszernek a választását, amely csak azon betegek számára hatékony, akiknél a HER2 expresszióját lehet igazolni a tumor szövetben. Más esetekben a többes biomarkerek egyidejű vizsgálata segít a betegség menedzsmentben. Pl. a „Tissue of Origin” teszt 1550 mRNS egyidejű expressziós mintázatának vizsgálatával segít a primer tumor keresésében.
|
|